
助力生物藥研發,淺談ADC藥物DAR值測定
導語
從上世紀初德國醫學家、諾貝爾獎得主Paul Ehrlich(保羅埃爾利希)提出ADC(Antibody-Drug Conjugate,抗體藥物偶聯物)的概念至今,ADC藥物已經發展至第三代,一系列特異性偶聯技術使得生產工藝變得更加穩定,能夠得到穩定藥抗比的藥物,對于ADC藥物的療效和安全性都有很大的貢獻,推動了ADC藥物的研發。抗體藥物偶聯物ADC是具有靶向作用的單克隆抗體與具有特定藥理學特性(如細胞毒作用)的化合物的結合,兩部分通過連接子偶聯為一個整體。DAR(Drug-to-Antibody Ratio,藥物抗體比值)是抗體藥物偶聯物的一個關鍵屬性,是ADC藥物研發過程重要的質控環節。
ADC藥物
帶您了解DAR值如何檢測
ADC藥物從本質上講是混合物,是由連接不同個數小分子藥物的單抗組成,DAR代表的是每個單抗上連接小分子藥物的平均數量,DAR直接影響ADC藥物的療效和安全性,藥物研發階段應盡量縮小DAR值的變動區間。
ADC藥物的偶聯位點分為單抗賴氨酸殘基上的氨基和半胱氨酸殘基上的巰基。通過賴氨酸偶聯的DAR往往比較小,而潛在的偶聯位點卻很多,偶聯反應具有隨機性,產物異質性較大;ADC藥物研發使用的單抗有4對鏈間二硫鍵,抗體通過部分還原使鏈間二硫鍵轉換成游離的半胱氨酸殘基,半胱氨酸殘基中的巰基與連接子中的馬來酰亞胺基反應形成ADC,一般連接的小分子數量為0、2、4、6和8,如圖所示。
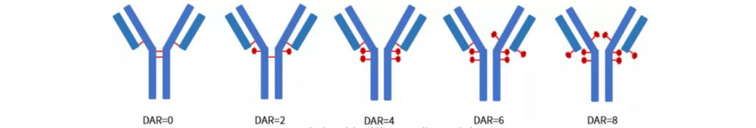
半胱氨酸偶聯的ADC藥物DAR分布
DAR測定的方法有多種,可分為光譜法、色譜法和質譜法,可根據ADC的特性及偶聯工藝等因素選擇合適的方法,具體如下:
紫外/可見光譜法(UV/Vis)
紫外/可見光譜法是檢測DAR值最簡單穩定的方法,這種方法需要抗體和小分子藥物具有不同的最大吸收波長,分別計算二者的濃度進而得到ADC的DAR值,適用于多種ADC。
色譜法
色譜法包括疏水作用色譜(HIC)和反相高效液相色譜法(RP-HPLC)兩種,適用于測定半胱氨酸偶聯的ADC。疏水作用色譜法能將不同DAR值的組分根據疏水性的差異分離開,且保持ADC分子的結構完整性;反相高效液相色譜法需要先將抗體還原得到輕、重鏈再進行分析,可用于補充驗證疏水作用色譜法的結果,并且適用于質譜分析。
質譜法
質譜法適用于賴氨酸偶聯的ADC的DAR值測定,包括液相色譜串聯質譜和MALDI-TOF-MS。賴氨酸偶聯的ADC具有較強的異質性,增加了質譜譜圖解析的難度,通常在測定前需對ADC進行額外的前處理,如去糖基化和去除C端賴氨酸異質性。
我們能做什么?
疏水作用色譜法解決方案
我們使用生物兼容液相系統(Nexera Bio)建立了一種疏水作用色譜方法用于抗體藥物偶聯物(ADC)中藥物抗體比值(DAR)和藥物分布的測定。

生物兼容液相系統(Nexera Bio)
Nexera Bio系統通過對關鍵部位的惰性化升級,在耐受高壓的前提下,升級的惰性表面降低了生物大分子在管路進樣針、檢測器中的吸附,并且可耐受高鹽洗脫體系,更適合于生物大分子樣品的分析。通過梯度洗脫,降低鹽濃度,增加有機相比例,可將偶聯不同藥物數量的ADC分離,未偶聯藥物的抗體疏水性最弱,最先被洗脫,連接8個藥物的抗體疏水性最強,最后被洗脫。峰面積百分比代表特定藥物數量連接的ADC的相對分布。通過峰面積百分比和偶聯藥物數量計算加權平均DAR。
我們將此方法應用于實際藥物的分析,并進行了重復性考察,發現液相系統穩定,方法重復性良好。
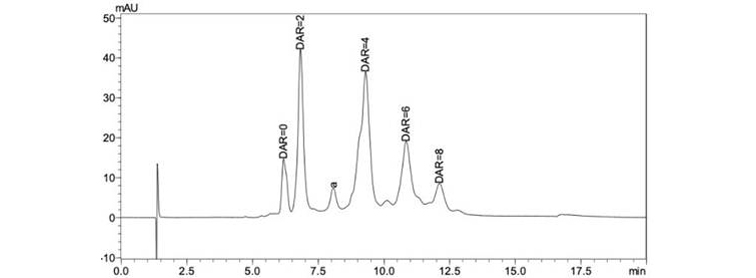
實際樣品色譜圖
表1. 藥物負荷分布和平均DAR值計算結果
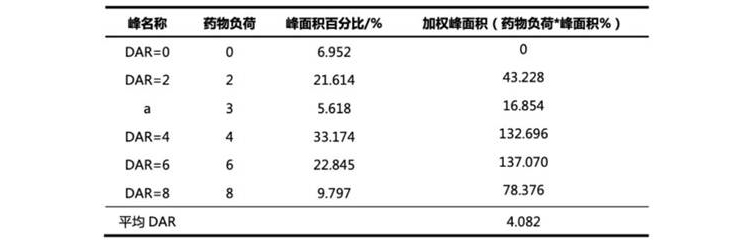
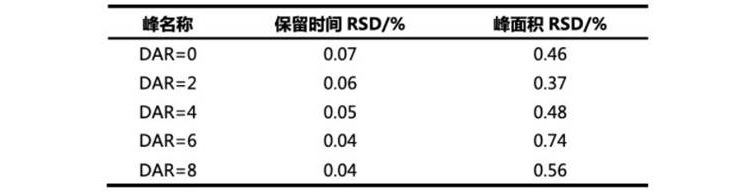
表2. 6次進樣數據重復性結果
我們還能做什么?
島津的產品線比較全面,包括紫外-可見吸收光譜、高效液相色譜、LCMS-Q-TOF以及MALDI-TOF質譜,可滿足不同用戶對于儀器的需求,較全面覆蓋ADC藥物DAR值測定以及其它生物制品的研發質控。




結語
經歷了幾十年的發展,ADC藥物研究取得了巨大進展,已上市藥物數量達到了12個,在研管道300多種。無論是賴氨酸偶聯還是半胱氨酸偶聯的ADC藥物,都是復雜的混合藥物,應該通過工藝的改進更好地控制DAR值變動區間,降低ADC藥物的異質性。島津一直關注生物藥行業的發展,希望以我們的儀器平臺為產品研發助力,推動新藥安全、有效地走向臨床,造福社會。


