
USP亞硝胺新通則<1469>大局已定,來了解一下吧

美國藥典(USP)擬定新通則
建議相關(guān)的原料藥/制劑/輔料生廠商和供應(yīng)商、合同制生產(chǎn)組織、藥品檢測和監(jiān)管機(jī)構(gòu)、QA/QC專家參考該通則。
USP
與FDA一樣,USP
原料藥工藝過程:原料、試劑、溶劑、加工助劑等
原料藥降解物
溶劑降解物
來自于原料、溶劑(回收溶劑)、試劑、催化劑的雜質(zhì)
來自于中間體和中間體生產(chǎn)帶來的雜質(zhì)
來自于水、輔料、加工助劑的雜質(zhì)
制劑加工或包裝材料引入或產(chǎn)生的雜質(zhì)
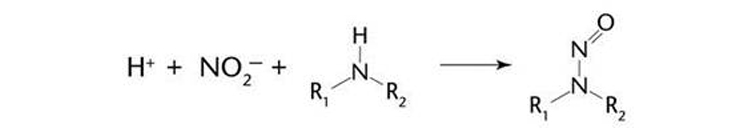
亞硝胺雜質(zhì)的產(chǎn)生機(jī)理
此外USP
通則要求單個亞硝胺雜質(zhì)不超過AI對應(yīng)的限度,同時對檢出濃度超過LOQ但不超過AI對應(yīng)限度的多個雜質(zhì)需咨詢權(quán)威機(jī)構(gòu)。筆者注:建議參考FDA的要求。
為了幫助供應(yīng)商更好地檢測亞硝胺雜質(zhì),USP
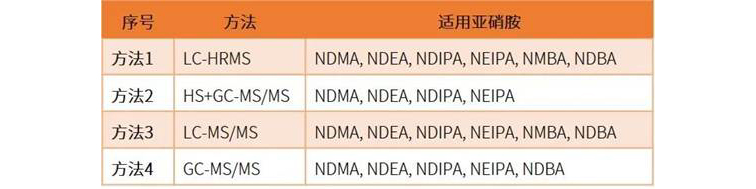
與EP 2.5.42僅限于原料藥不同,USP
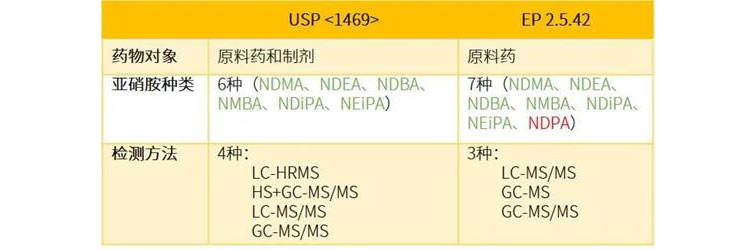
島津可以為客戶提供USP

關(guān)于USP
應(yīng)用案例1
島津海外應(yīng)用工程師參考USP
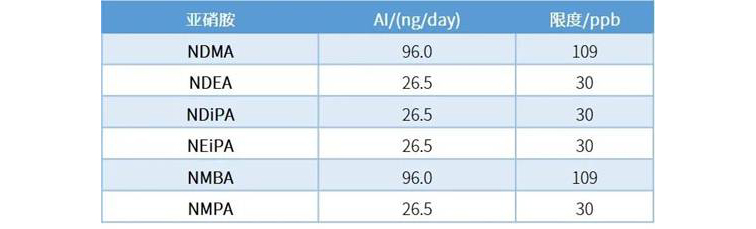
使用島津HS-20和GC-MS/MS對方法進(jìn)行研究,考察線性、準(zhǔn)確度(回收率)、LOQ等參數(shù),結(jié)果如下:
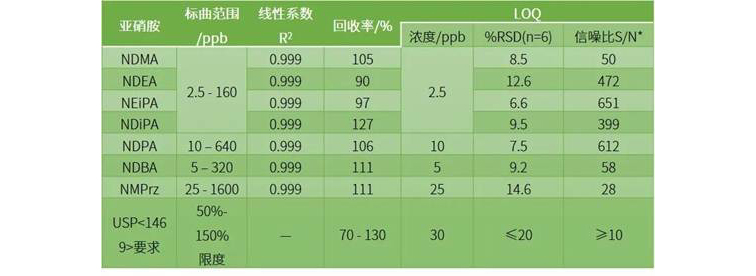
實(shí)驗(yàn)結(jié)果表明,島津儀器性能超越了USP
應(yīng)用案例2
參考
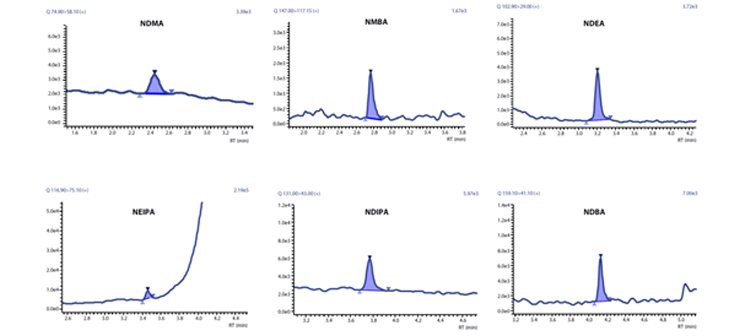
0.1ng/mL亞硝胺的MRM質(zhì)量色譜圖
數(shù)據(jù)展示:0.1 ng/mL 標(biāo)準(zhǔn)溶液的MRM色譜圖如上圖(該濃度是FDA要求的定量限值的 1/10)。在0.1 - 10 ng/mL濃度范圍內(nèi)的線性系數(shù)>0.99,該濃度范圍內(nèi)的精密度在80 - 120%,結(jié)果優(yōu)異。
更多應(yīng)用信息請聯(lián)絡(luò)島津工作人員!


